Am Pösenberg 9-13
D-41517 Grevenbroich
Telefon: +49 2181 70 676 - 0
Fax: +49 2181 70 676 - 22
E-Mail senden
SALINACIÓN EXCESIVA
Ácidos húmicos pueden reducir el problema de salinización de tierras de cultivos, especialmente en regiones que han sufrido demasiado riego superficial han dado lugar a toxicidades. En suelos afectados por el exceso de salinización, los ácidos húmicos pueden sanear aniones y cationes y eliminarlos de la región de las raíces de las plantas y proporcionar una compensación para el déficit de sustancias orgánicas.
Uno de los mejores ejemplos de salinización excesiva ha sido observada en Egipto con la construcción de la presa de Assuan en 1970, que intervino en el flujo natural del río Nilo. Una de las consecuencias fue la eliminación de los complejos arcilla-humáticos del río como fertilizantenatural, ya que suministraba nutrientes y ácidos húmicos. Otro efecto fue la salinización de los suelos a través de un nivel igualmente alto de agua subterránea. Por eso, Egipto se convirtió mundialmente en uno de los mayores importadores de fertilizantes en sólo unos 10 años. Por la reducción de velocidad de flujo del Nilo llevó se acumularon los nutrientes esenciales para los suelos fértiles en el lago de la presa y, a consecuencia, eso produjo un enorme déficit de nutrientes en las tierras de cultivo.
 image of Highly salinized soil
image of Highly salinized soil
foto 1: Suelo altamente salinizado.
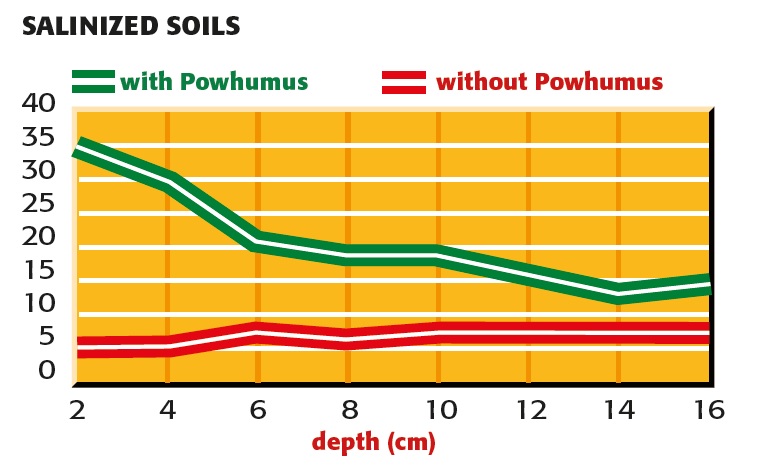 Splitting of salt with and without powhumus
Splitting of salt with and without powhumus
fig.1: Suelo altamente salinizado.
Los constantes cambios en el nivel de las aguas subterráneas antes de la construcción de la presa habían permitido una continua erosión del suelo, lo que garantizaba que no había una concentración de aniones y cationes indeseados en las capas superiores. Con un nivel alto continuo de agua subterránea seguida después de la construcción de la presa, este tipo de concentración ocurrió efectivamente. A consecuencia de la salinización y alcalinización de los suelos condujo naturalmente a pérdidas en los rendimientos de cultivos e incluso a un abandono total de tierras cultivables.
Este tipo de intervención radical en el sistema ecológico ha tenido consecuencias similares en otros países. Iones responsables de la salinización son:
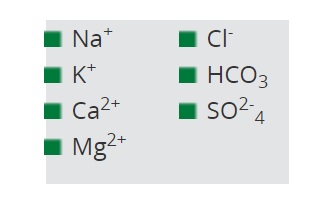 chemicals for which humic acids have fixation properties
chemicals for which humic acids have fixation properties
Investigaciones han demostrado que ácidos húmicos tienen propiedades de fijación para lo siguiente:
- Iones Na+ y Cl- están ligados por ácidos húmicos.
- NaHCO3 es adsorbido después de la isoterma tipo L.
- La fijación de Mg2 + y Ca2 + por ácidos húmicos se sabe hace mucho tiempo.
Por un lado, estas sales son adsorbidas por la superficie de los ácidos húmicos, y, por otro lado, susiones también pueden fijarse electros- ticamente por los correspondientes grupos funcionales (grupos carboxilo y grupos OH).
La propiedad de los ácidos húmicos de formar complejos con cationes polivalentes es de gran importancia aquí. Sales con iones bivalentes se fijan con más fuerza de lo esperado. Más significativo es, que este tipo de fijación (adsorción) tiene lugar relativamente con poca energía, lo cual produce una interrupción en el equilibrio con el hundimiento del agua subterránea durante las fases secas y por lo tanto resulta en una liberación de iones y sus enlaces a las capas más profundas de la tierra de nuevo a su lugar original.
1. Fixación de iones metálicos (Me+):
2. Fijación de aniones: ácidos húmicos como bases:
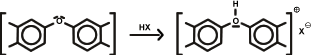 Fixation of anions: humic acids as bases
Fixation of anions: humic acids as bases
Reducción demostrada en salinización de suelos en Egipto a través de ácidos húmicos:
I. Estado de los suelos antes de la construcción de la Presa de Assuan
Liberación de sales de las capas más profundas del suelo, con aguas subterráneas hundidas: llevadas de vuelta a las capas más profundas del suelo.
II.1 Estado de suelos después de la construcción de la Presa de Assuan sin ácidos húmicos
Fuera de la cristalización de sales en el horizonte superior con acumulación permanente: salinización
II.2 Estado del suelo después de la construcción de la presa de Assuan en presencia de ácidos húmicos
Fijación de iones (1) y balance de solubilidad (2). Los pequeños ácidos húmicos móviles actúan como barrera en las capas superiores: sin salinización (3).
Parte de la información en esta página se derivó de Wolfgang Ziechmann, Huminstoffe und ihre Wirkungen, Spektrum Akademischer Verlag, Heildelberg - Berlin - Oxford, 1996.
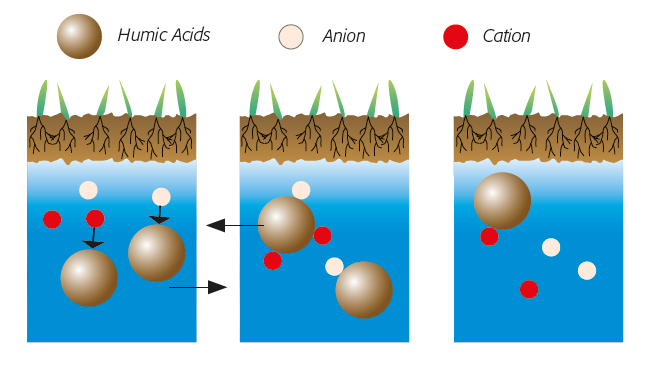 depiction of how Humic acids reduce the effects of salinity
depiction of how Humic acids reduce the effects of salinity
fig.2: Los ácidos húmicos reducen el efecto de la salinidad.
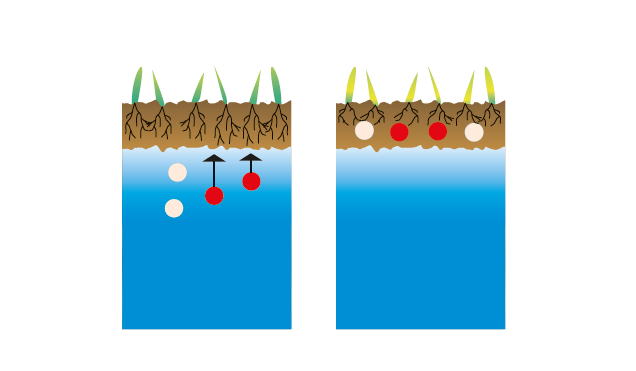
fig.3: Agua subterránea salinizada en un suelo.


